A ocorrência de doenças hepáticas e cardíacas terminais de maneira conjunta, seja pela mesma ou diversas etiologias pode demandar a realização de um transplante coração-fígado combinado (TCFC). O primeiro TCFC foi descrito por Starlz em 1984(1) e até 2015 foram realizados 190 nos Estados Unidos(2) e 45 na França(3).
A indicação mais comum do TCFC é a polineuropatia amiloidótica familiar (PAF). Nessa doença há acúmulo de proteínas anormais em vários locais do organismo, sendo que no coração leva eventualmente à insuficiência cardíaca. Nesses casos, a realização concomitante do transplante hepático tem o intuito de prevenir a deposição dessas proteínas anormais no coração transplantado.
Os fígados retirados de portadores de PAF podem eventualmente ser utilizados em outros receptores bem selecionados, em uma modalidade chamada transplante dominó.
Das etiologias hepáticas envolvidas no transplante combinado ganha destaque a hepatopatia congestiva ou cirrose cardiogênica. A depender da etiologia da doença cardíaca a doença hepática pode cursar com os mesmos fatores de risco, como o álcool ou ação dos comemorativos da síndrome metabólica, cursando com a doença hepática gordurosa associada ao metabolismo (MAFLD).
O aumento da sobrevida dos pacientes operados por cardiopatia congênita e as consequências para a hemodinâmica hepática das cirurgias univentriculares (circulação de Fontan), tem levado a um aumento das indicações do transplante combinado para esses pacientes(4).
As particularidades da avaliação hepática.
Tendo como foco a doença hepática, a presença de cirrose é uma contra-indicação ao transplante cardíaco isolado para a maioria das equipes(3), ou seja, a presença de hipertensão portal é um fator que resulta na necessidade de um transplante combinado(5). O diagnóstico da cirrose hepática no ambiente da doença cardiológica congestiva carrega alguns desafios. Em relação a avaliação morfológica – por tomografia/ultrassonografia/ressonância – armadilhas interpretativas podem limitar o valor preditivo positivo desses exames, em virtude de um órgão dismórfico ser resultado de hiperplasia nodular regenerativa, ascite ser decorrente de hipertensão portal pós-sinusoidal (dificuldade outflow pela insuficiência cardíaca) ou a própria hepatomegalia congestiva.
A disponibilização de métodos não invasivos de quantificação de fibrose – elastografia – tem reconhecidas limitações na presença de ascite, assim como uma reconhecida superestimação da fibrose nos casos de congestão hepática(3).
Para avaliação morfológica acaba restando a definição por biópsia hepática, com seus riscos inerentes e amplificados pela doença de base, sendo que sua utilização não atinge o consenso nas indicações dos transplantes combinados. O achado histológico clássico é a fibrose de origem centrilobular(6, 7), quando essa se estende a região periportal já nos deparamos com doença mais avançada(8, 9).
A avaliação funcional da capacidade sintética hepática tem seus problemas quando consideramos que os escores normalmente utilizados para esse fim, como o model for end-stage liver disease (MELD) e o Child-Turcotte-Pugh (CHILD) são indiretos e seus compostos matemáticos (bilirrubina, sódio, RNI, creatinina, albumina) podem estar alterados em um contexto de doença cardiológica ou renal associada.
O que a literatura nos acrescenta.
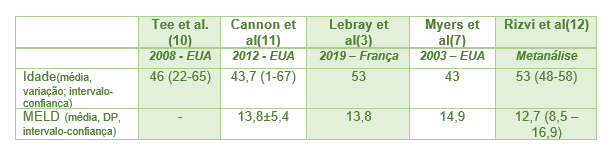
Das séries de análises de casos ou de estudos multicêntricos na Europa e Estados Unidos observamos na tabela abaixo, que em média de idade esses transplantes se situam entre a quarta e quinta década de vida, com escore de gravidade MELD em torno de 15.
Em relação à técnica cirúrgica a maioria dos centros realiza o transplante combinado em dois tempos distintos, constituindo-se primeiro a realização do transplante cardíaco, saída da circulação extra-corpórea, término da anti-coagulação e realização do transplante hepático(2).
A realização de ambos os transplantes em vigência de circulação extra-corpórea, apesar de não mais ser a estratégia padrão, tem seus defensores em razão de uma potencial melhor estabilidade hemodinâmica e redução do estresse metabólico ao novo coração; sendo que questões relacionadas ao impacto da reperfusão simultânea(13) ou do período requerido para a reversão da anti-coagulação(14) não tem respostas precisas.
Em relação à tática imunossupressora, interessantes questões imunológicas são resultantes do papel do fígado com um indutor de tolerância, relacionadas ao microquimerismo, deleção ou regulação de células T e neutralização de anticorpos derivados do doador(5). Essas particularidades resultam numa tolerância melhor a níveis mais baixos de imunossupressores, com menor risco de rejeição do aloenxerto cardíaco(10, 15).
Em uma metanálise que demonstrou taxas menores de rejeição(12), referências aos esquemas de imunossupressão não foram abdordados, somente o desfecho reportado de eventos de rejeição, o mesmo observado em uma revisão da base de dados da United Network of Organ Sharing do Estados Unidos(15). A busca pelos trabalhos de centro único que contemplam em seus métodos a terapia imunossupressora demonstram a utilização de: OKT3 seguido de inibidor de calcineurina e corticóide(16); corticóide, micofenolato e tacrolimus com(17) ou sem indução(16-19) com timoglobulina.
De um ponto de vista da alocação de órgãos, a legislação brasileira contempla o transplante combinado coração-figado utilizando o status cardíaco(20), na alocação do coração o fígado é distribuído em conjunto com ele.
Considerações finais.
O transplante combinado de coração e fígado tem suas particularidades de uma indicação adequada, apoio técnico cirúrgico e imunológico adequado. Inexiste na literatura os melhores graus de evidência nesse tipo de indicação de transplante pouco comum. O melhor julgamento multidisciplinar deve ser buscado caso-a-caso.
Referências bibliográficas.
Starzl TE, Bilheimer DW, Bahnson HT, Shaw BW, Jr., Hardesty RL, Griffith BP, et al. Heart-liver transplantation in a patient with familial hypercholesterolaemia. Lancet. 1984;1(8391):1382-3.
Beal EW, Mumtaz K, Hayes D, Jr., Whitson BA, Black SM. Combined heart-liver transplantation: Indications, outcomes and current experience. Transplant Rev (Orlando). 2016;30(4):261-8.
Lebray P, Varnous S. Combined heart and liver transplantation: State of knowledge and outlooks. Clin Res Hepatol Gastroenterol. 2019;43(2):123-30.
Gong T, Hall S. Considerations and experience driving expansion of combined heart-liver transplantation. Curr Opin Organ Transplant. 2020;25(5):496-500.
Yi SG, Lunsford KE, Bruce C, Ghobrial RM. Conquering combined thoracic organ and liver transplantation: indications and outcomes for heart-liver and lung-liver transplantation. Curr Opin Organ Transplant. 2018;23(2):180-6.
Horvath B, Zhu L, Allende D, Xie H, Guirguis J, Cruise M, et al. Histology and Glutamine Synthetase Immunoreactivity in Liver Biopsies From Patients With Congestive Heart Failure. Gastroenterology Res. 2017;10(3):182-9.
Myers RP, Cerini R, Sayegh R, Moreau R, Degott C, Lebrec D, et al. Cardiac hepatopathy: clinical, hemodynamic, and histologic characteristics and correlations. Hepatology. 2003;37(2):393-400.
Bosch DE, Koro K, Richards E, Hoch BL, Jalikis F, Koch LK, et al. Validation of a Congestive Hepatic Fibrosis Scoring System. Am J Surg Pathol. 2019;43(6):766-72.
Dai DF, Swanson PE, Krieger EV, Liou IW, Carithers RL, Yeh MM. Congestive hepatic fibrosis score: a novel histologic assessment of clinical severity. Mod Pathol. 2014;27(12):1552-8.
Te HS, Anderson AS, Millis JM, Jeevanandam V, Jensen DM. Current state of combined heart-liver transplantation in the United States. J Heart Lung Transplant. 2008;27(7):753-9.
Cannon RM, Hughes MG, Jones CM, Eng M, Marvin MR. A review of the United States experience with combined heart-liver transplantation. Transpl Int. 2012;25(12):1223-8.
Rizvi SSA, Challapalli J, Maynes EJ, Weber MP, Choi JH, O’Malley TJ, et al. Indications and outcomes of combined heart-liver transplant: A systematic review and met-analysis. Transplant Rev (Orlando). 2020;34(2):100517.
Detry O, Honore P, Meurisse M, Defraigne JO, Defechereux T, Sakalihasan N, et al. Advantages of inferior vena caval flow preservation in combined transplantation of the liver and heart. Transpl Int. 1997;10(2):150-1.
Rauchfuss F, Breuer M, Dittmar Y, Heise M, Bossert T, Hekmat K, et al. Implantation of the liver during reperfusion of the heart in combined heart-liver transplantation: own experience and review of the literature. Transplant Proc. 2011;43(7):2707-13.
Chou AS, Habertheuer A, Chin AL, Sultan I, Vallabhajosyula P. Heart-Kidney and Heart-Liver Transplantation Provide Immunoprotection to the Cardiac Allograft. Ann Thorac Surg. 2019;108(2):458-66.
Raichlin E, Kushwaha SS, Daly RC, Kremers WK, Frantz RP, Clavell AL, et al. Combined heart and kidney transplantation provides an excellent survival and decreases risk of cardiac cellular rejection and coronary allograft vasculopathy. Transplant Proc. 2011;43(5):1871-6.
Careddu L, Zanfi C, Pantaleo A, Loforte A, Ercolani G, Cescon M, et al. Combined heart-liver transplantation: a single-center experience. Transpl Int. 2015;28(7):828-34.
Atluri P, Gaffey A, Howard J, Phillips E, Goldstone AB, Hornsby N, et al. Combined heart and liver transplantation can be safely performed with excellent short- and long-term results. Ann Thorac Surg. 2014;98(3):858-62.
Hermsen JL, Nath DS, del Rio AM, Eickstaedt JB, Wigfield C, Lindsey JD, et al. Combined heart-kidney transplantation: the University of Wisconsin experience. J Heart Lung Transplant. 2007;26(11):1119-26.
Portaria de Consolidação nº4, de 28 de setembro de 2017., (2017)
Aviso legal: como médicos também temos a função social de divulgar a medicina e saúde, aproveite essas informações para cuidar da sua. Entretanto, reforçamos que ela não substitui atendimento médico.

Médico pela PUCPR (CRM 20009/PR). Residência médica em cirurgia geral pela PUCPR, com área de atuação em cirurgia vídeo-laparoscópica (RQE 192). Título de Especialista em Cirurgia Geral pelo Colégio Brasileiro de Cirurgiões (RQE 13560). Título de Especialista em Cirurgia do Aparelho Digestivo pelo Colégio Brasileiro de Cirurgia Digestiva (RQE 15509). Atua na área de transplante de fígado, pâncreas e rim. Membro da Associação Brasileira de Transplante de Órgãos (ABTO), da Sociedade Internacional de Transplante de Fígado (ILTS) e da Sociedade de Transplantação (TTS).


